エクソソーム(Exosome、エキソソームとも呼ばれる)は細胞から分泌される直径50-150 nm(ナノメートル:10億分の1メートル)の顆粒状の物質です。その表面は細胞膜由来の脂質、タンパク質を含み、内部には核酸(マイクロRNA、メッセンジャーRNA、DNAなど)やタンパク質など細胞内の物質を含んでいます。エクソソームは細胞外小胞(Extracellular vesicle)の一種とされており、細胞外小胞にはエクソソームのほかにマイクロベシクル、アポトーシス小体があり、それぞれ産生機構や大きさが異なります(図1)。
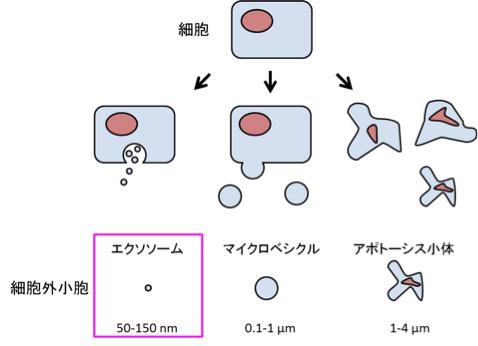
図1【エクソソームは細胞外小胞の1つである】
細胞外小胞は産生機構や大きさによってエクソソーム、マイクロベシクル、アポトーシス小体に大きく分類される。エクソソームはエンドソーム由来の小胞、マイクロベシクルは細胞から直接分泌された小胞、アポトーシス小体は細胞死により生じた細胞断片である。 (μm:マイクロメートル、100万分の1メートル)
エクソソームは、エンドサイトーシス(細胞が細胞外の物質を取り込む機構の一種)により細胞内にできたエンドソームがさらに陥入することで作られた膜小胞が、細胞外に放出されたものです(図2)。エクソソームの表面には細胞膜成分が、内部には細胞内の物質が含まれるため、分泌された元の細胞の特徴を反映していると考えられています。
エクソソームには共通に含まれるタンパク質があります。表面にはテトラスパニン類(CD9、CD63、CD81など)やインテグリン類などの膜タンパク質、主要組織適合遺伝子複合体(MHC)分子が、また内部には多胞体形成に関連するタンパク質(Tsg101、Alix)、熱ショックタンパク質(HSP)が多く存在することが知られています(図3)。このことからCD9など表面に存在するタンパク質を利用してエクソソームを回収する試みも行われています。
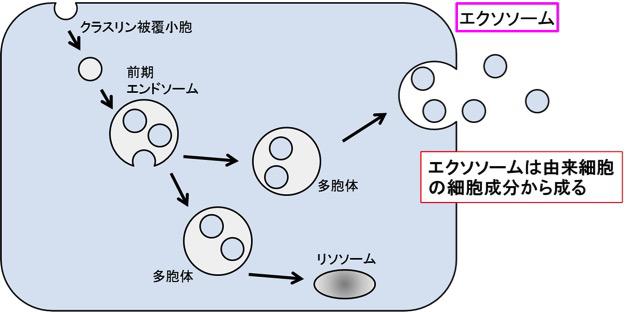
図2【エクソソームのできかた】
エクソソームはエンドソーム内に作られる膜小胞が細胞外に分泌されたものである。
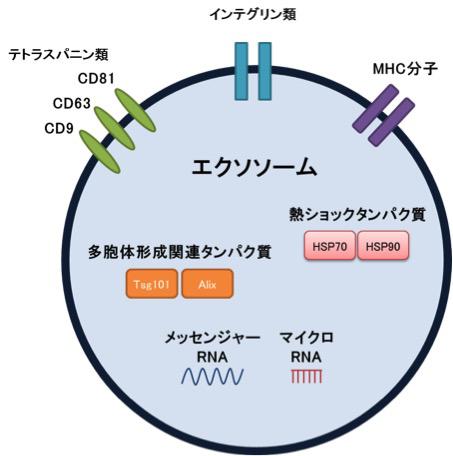
図3【エクソソームに共通して含まれるタンパク質など】
エクソソームには共通して含まれているとされるタンパク質がいくつかある。また、エクソソームは細胞内のタンパク質、核酸などを含むため、由来する細胞の特徴を反映していると考えられている。
細胞から分泌されたエクソソームは細胞と細胞の間に存在するだけでなく、体液(血液、髄液、尿など)にも存在しており、体中を循環しています。エクソソームの重要な機能として注目されているのは、細胞間の情報伝達に使われているということです。前述のようにエクソソームはその内部に核酸、タンパク質などを含んでいます。分泌した細胞の核酸(マイクロRNA、メッセンジャーRNA)がエクソソームを介して受け取り側の細胞に伝達され、機能していることが報告された(文献1)ことから、エクソソームは細胞間のコミュニケーションツールとして働いていると考えられています(図4)。最近では、悪性度の高いがん細胞から放出されたエクソソームが悪性度の低い細胞に働きかけ、その細胞の性質を変化させることを証明した報告も出ています(文献2)。
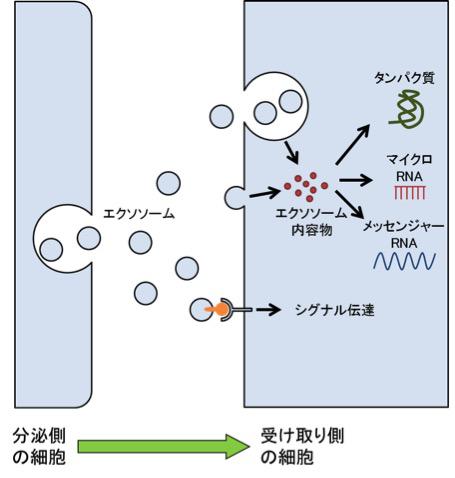
図4【エクソソームは細胞間のコミュニケーションに使われる】
分泌されたエクソソームが受け取り側の細胞の表面にある受容体に作用してシグナル伝達を引き起こすことや、細胞内部に取り込まれたエクソソームの内容物が受け取り側の細胞で機能することが考えられている。
近年、エクソソームは様々な病気に関わっていることが示唆されています。その代表が「がん」との関係で、がん細胞から放出されるエクソソームはがん細胞の生存、悪性化、転移などに関与し、がん細胞に有利に働くように機能していると考えられています(図5)。例えば、マウスに肺転移性のがん細胞由来のエクソソームを事前に静脈投与して、その後骨転移性のがん細胞を静脈投与すると細胞自体には肺転移能がないにもかかわらず、エクソソームの事前投与により肺への転移が増加することが報告されています(文献3)。また、神経変性疾患(アルツハイマー病など)など、がん以外の病気とエクソソームとの関係も報告されています。
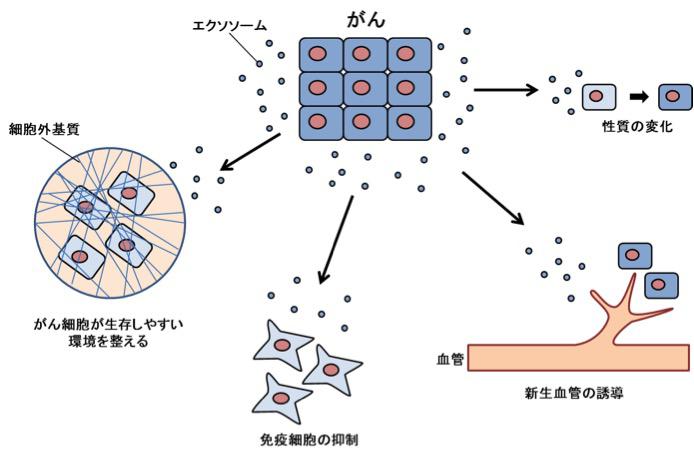
図5【がん細胞が出すエクソソームは、がんの生存に有利に働く】
がん細胞から分泌されるエクソソームは、がんが生存しやすいように細胞外の環境を整える、免疫細胞を抑制する、新生血管を誘導する、さらには他の細胞の性質を変化させるものと考えられている。
細胞から分泌されるエクソソームは分泌元の細胞の特徴を反映しているのに加えて、体液中に存在していることから、病気の診断に使えるのではないかと注目を集めています。体液中のがん細胞やその由来成分による診断はリキッドバイオプシー(Liquid Biopsy)と呼ばれ、エクソソームも診断マーカーとして期待されています(図6)。
例を挙げると、国内では国立がん研究センターが血中のCD147/CD9陽性エクソソームによる大腸がんの早期診断法を開発したとの報告がなされています(文献4)。海外ではExosome Diagnostics社がエクソソーム中のRNAを利用した体液診断法の開発を進めています(文献5)。このように国内外の様々な研究機関、企業がエクソソームを利用した病気の診断法の開発に取り組んでいます。
私たちも前立腺特異的な膜表面タンパク質に対する抗体を利用することで前立腺特異的エクソソームを回収することができることを報告しています(文献6)。現在、前立腺がん患者で、前立腺特異的エクソソームを用いた前立腺がんマーカーの検出とその臨床応用に向けた研究を進めています。
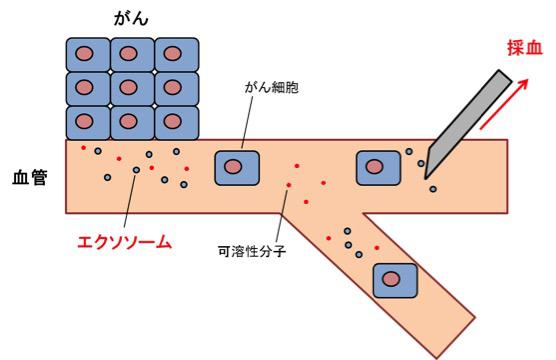
図6【リキッドバイオプシー】
がん患者の血中には、がん細胞、がん細胞から分泌される可溶性分子、エクソソームなどが存在している。体液中を循環しているこれらを検出することで病気を診断するというのがリキッドバイオプシーである。
一方、エクソソームが内包する物質を安定的に輸送するという細胞間情報伝達ツールとしての機能に着目し、治療標的細胞への薬剤の輸送(ドラックデリバリーシステム)への利用にも注目が集まっています。実際に、がんに対する薬剤や核酸を封入させたエクソソームを投与することにより、がんが縮小することなどが動物実験で示されています。
以上、エクソソームは分泌元の細胞の情報を反映し、細胞間情報伝達機能を有することから、それを標的とした診断、治療まで様々な分野への応用の可能性があります。エクソソームの研究はこれからますます発展していくことが予想されており、私たちは様々な可能性を視野に入れ、細胞間情報伝達物質としてのエクソソームの機能および疾患マーカーとしてのエクソソーム評価法の開発に関する研究を行っています。